
Cardiotoxicidad en tratamientos oncológicos II
El tratamiento del cáncer ha tenido una evolución espectacular, los pilares de su tratamiento han experimentado gran sofisticación en los últimos años. Aunque experimentan eventos adversos y entre ellos la cardiotoxicidad es uno de gran importancia. En el anterior blog analizamos la cardiotoxicidad de algunos tratamientos y a continuación detallaremos los efectos de otros tratamientos, en el presente caso nos enfocaremos en los anticuerpos monoclonales, así como inmunoterapia en relación a cardiotoxicidad.
Anticuerpos monoclonales
Es clásico el hallazgo de inmunoglobulinas monoclonales en pacientes con mieloma múltiple y que demostraron actividad inhibitoria como los describió Itoh de la Universidad de Tohoku en el año 19681. Posteriormente en los años 70 la identificación de los primeros blancos moleculares en células neoplásicas se constituyó en el inicio de esta apasionante carrera de desarrollo de nuevas terapias; como ejemplo tenemos la identificación de marcadores de membrana en leucemias y linfomas2 o el estudio de anticuerpos producido por células híbridas contra el melanoma3; el siguiente paso por esta senda se produce en los años 80 con el ensayo de anticuerpos monoclonales, es menester el mencionar el estudio fase I de Sears con anticuerpo murino que inhibía el crecimiento de tumores gastrointestinales en 4 pacientes; 3 de ellos desarrollaron anticuerpos contra el monoclonal murino4; para el año 1983 Oldham realiza una revisión de la experiencia científica relacionada a anticuerpos monoclonales, es llamativo que entre los efectos adversos ya se menciona la aparición de disnea, hipertensión o hipotensión lo que muestra un efecto cardiovascular de estas terapias5. Desde allí hasta la fecha, amplio ha sido el caudal que ha pasado bajo el puente de la terapéutica del cáncer; hasta la fecha en PUBMED encontramos 5,057 publicaciones de anticuerpos monoclonales y cáncer entre estudios de fase II, III y IV6; sin embargo, si buscamos que publicaciones además de lo anterior abarcan cardiotoxicidad el número se reduce drásticamente a 78 y en el siguiente gráfico veremos la relación entre los dos tipos de búsqueda:
Gráfico 1: Comparación de estudios con la búsqueda: “estudios clínicos con anticuerpos monoclonales y cáncer” versus “estudios clínicos con anticuerpos monoclonales en cáncer y cardiotoxicidad”6,7.
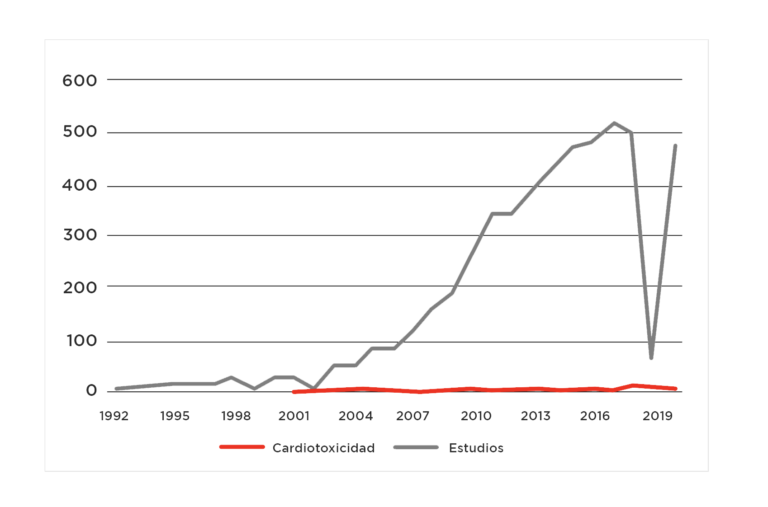
La diferencia es abismal, sin embargo, si hacemos la búsqueda enfocados en uno de los efectos cardiovasculares que más relevancia se ha encontrado en este tipo de tratamiento cómo es la hipertensión se encuentra algo más de publicaciones:
Gráfico 2: Comparación de estudios con la búsqueda: “estudios clínicos con anticuerpos monoclonales y cáncer” versus: “estudios clínicos con anticuerpos monoclonales en cáncer y cardiotoxicidad” y versus: “estudios clínicos con anticuerpos monoclonales en cáncer e hipertensión”6,7,8.
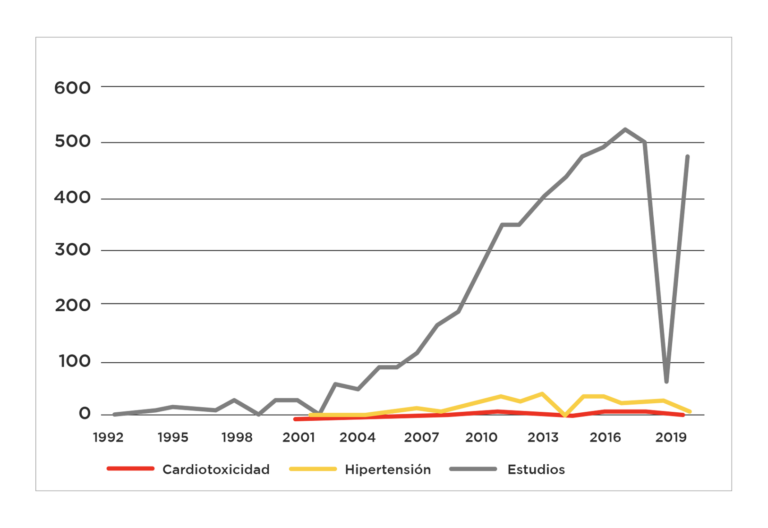
Ahora si hacemos una revisiones que en los términos de búsqueda incluyan diversos tipos de trastornos cardiacos encontramos gran disparidad entre los reportes, por ejemplo observamos que no hay tendencia de crecimiento como lo hay algo más marcada en los estudios de forma global; además encontramos que la búsqueda de cardiotoxicidad no equivale a problemas como hipertensión o insuficiencia cardiaca lo que muestra la disparidad de los reportes de eventos relacionados al sistema cardiovascular y que implica que esta área tiene mucho por desarrollar.
Gráfico 3: Comparación de estudios con la búsqueda: “estudios clínicos con anticuerpos monoclonales y cáncer” comparando a los términos adicionales: cardiotoxicidad, insuficiencia cardiaca, hipertensión, infarto e hipotensión6,7,8,9,10,11.
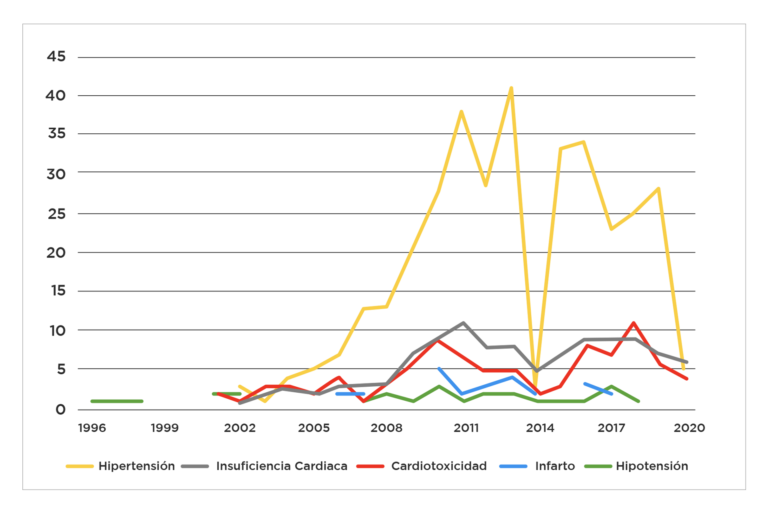
Para cerrar el presente blog mencionaremos a continuación los efectos de anticuerpos vigentes para tratamiento de cáncer aprobados por la FDA y filtrados por la situación de registro a nivel nacional. Hay que mencionar que hasta el año 2020 F.D.A. ha aprobado 23 anticuerpos no conjugados y 12 anticuerpos conjugados para el cáncer, en Ecuador están registrados 11 anticuerpos no conjugados (47,8% de los aprobados en E.E.U.U.) y 4 conjugados (36,4% de los aprobados en E.E.U.U.) y se detallan a continuación12,13.
Tabla 1: Anticuerpos monoclonales aprobados hasta 2020 por F.D.A. para cáncer y registrados en Ecuador12,13.

*Aprobación inicial por F.D.A. (Food and Drug Administration).
¿Podría haber cardiotoxicidad con los anticuerpos monoclonales?
Hay evidencia de un incremento de riesgo con algunos de ellos, en el caso de trastuzumab, anticuerpo dirigido contra el HER2neu se ha encontrado un incremento en algunos estudios, sin embargo quisiera mencionar a la publicación de Cho, que analizó retrospectivamente a 613 pacientes en Corea del Sur. Se encontró que la adición de trastuzumab podría mostrar mayor cantidad de casos con cardiotoxicidad14.
Gráfico 3: Cardiotoxicidad acumulativa en el estudio retrospectivo de Cho en Corea14. (Tomado del artículo)
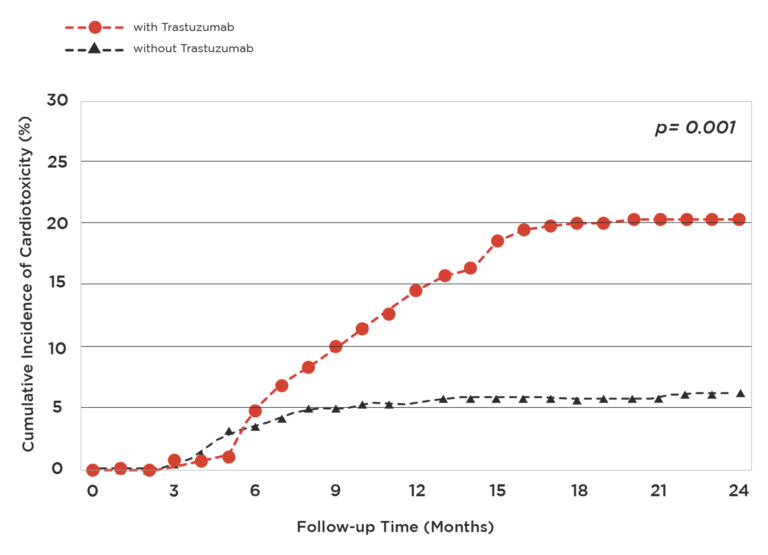
En el presente estudio se encuentra una tendencia que se incrementa hasta los 15 meses de seguimiento, qué factores predisponen para este problema, en el mismo estudio se detallan los siguientes:
Tabla 2: Factores de riesgo para cardiotoxicidad en pacientes con Cáncer de mama que reciben tratamiento en el estudio retrospectivo en Corea de Cho14.

Llama la atención que el paciente con metástasis presenta mayor riesgo, esto nos orienta en que el apoyo del cardiólogo es de importancia en este grupo de pacientes, con realce si recibirán trastuzumab o si además han recibido antraciclinas que sigue siendo el principal factor de riesgo de cardiotoxicidad. Sin embargo de esto uno podría considerar que al añadir un nuevo tratamiento cómo el pertuzumab elevaría los casos, el estudio de Gong en Ontario nos muestra que la incidencia de insuficiencia cardiaca con la combinación de trastuzumab y pertuzumab tiene un valor bajo de 1,8 por 100 personas/año y en el caso de TDM1 la incidencia es de 0,02 eventos persona/año15. Lo que muestra que en mundo real la interacción con sistemas que provean atención cardiológica podría marcar diferencias. Sin embargo hay aún camino por recorrer con estos tratamientos.
Bibliografía
1.- Itoh, C., Hashimoto, I., Onuma, Y. and Ishitoya, Y., 1968. Inhibitory Effects of Monoclonal Immunoglobulins on Anti-globulin Reaction. The Tohoku Journal of Experimental Medicine, 94(3), pp.307-313..
2.- Seligmann, M., 1976. Membrane cell markers in human leukemias and lymphomas. La Ricerca in Clinica e in Laboratorio, 6(2), pp.93-98..
3.- Koprowski, H., Steplewski, Z., Herlyn, D. and Herlyn, M., 1978. Study of antibodies against human melanoma produced by somatic cell hybrids. Proceedings of the National Academy of Sciences, 75(7), pp.3405-3409..
4.- Sears, H., Mattis, J., Herlyn, D., Häyry, P., Atkinson, B., Ernst, C., Steplewski, Z. and Koprowski, H., 1982. PHASE-I CLINICAL TRIAL OF MONOCLONAL ANTIBODY IN TREATMENT OF GASTROINTESTINAL TUMOURS. The Lancet, 319(8275), pp.762-765..
5.- Oldham, R., 1983. Monoclonal antibodies in cancer therapy. Journal of Clinical Oncology, 1(9), pp.582-590..
6.- PubMed. 2021. monoclonal antibody cancer – Search Results – PubMed. [online] Available at: <https://pubmed.ncbi.nlm.nih.gov/?term=monoclonal+antibody+cancer&filter=pubt.clinicaltrialphaseii&filter=pubt.clinicaltrialphaseiii&filter=pubt.clinicaltrialphaseiv&sort=date&sort_order=asc&size=200> [Accessed 18 May 2021].
7.- PubMed. 2021. monoclonal antibody cancer – Search Results – PubMed. [online] Available at: <https://pubmed.ncbi.nlm.nih.gov/?term=monoclonal+antibody+cancer+cardiotoxicity&filter=pubt.clinicaltrialphaseii&filter=pubt.clinicaltrialphaseiii&filter=pubt.clinicaltrialphaseiv&sort=date&sort_order=asc&size=200> [Accessed 18 May 2021].
8.- PubMed. 2021. monoclonal antibody cancer – Search Results – PubMed. [online] Available at: <https://pubmed.ncbi.nlm.nih.gov/?term=monoclonal+antibody+cancer+hypertension&filter=pubt.clinicaltrialphaseii&filter=pubt.clinicaltrialphaseiii&filter=pubt.clinicaltrialphaseiv&sort=date&sort_order=asc&size=200> [Accessed 18 May 2021].
9.- PubMed. 2021. monoclonal antibody cancer – Search Results – PubMed. [online] Available at: <https://pubmed.ncbi.nlm.nih.gov/?term=monoclonal+antibody+cancer+hypotension&filter=pubt.clinicaltrialphaseii&filter=pubt.clinicaltrialphaseiii&filter=pubt.clinicaltrialphaseiv&sort=date&sort_order=asc&size=200> [Accessed 18 May 2021].
10.- PubMed. 2021. monoclonal antibody cancer – Search Results – PubMed. [online] Available at: <https://pubmed.ncbi.nlm.nih.gov/?term=monoclonal+antibody+cancer+cardiac+failure&filter=pubt.clinicaltrialphaseii&filter=pubt.clinicaltrialphaseiii&filter=pubt.clinicaltrialphaseiv&sort=date&sort_order=asc&size=200> [Accessed 18 May 2021].
11.- PubMed. 2021. monoclonal antibody cancer – Search Results – PubMed. [online] Available at: <https://pubmed.ncbi.nlm.nih.gov/?term=monoclonal+antibody+cancer+infarction&filter=pubt.clinicaltrialphaseii&filter=pubt.clinicaltrialphaseiii&filter=pubt.clinicaltrialphaseiv&sort=date&sort_order=asc&size=200> [Accessed 18 May 2021].
12.- Permisosfuncionamiento.controlsanitario.gob.ec. 2021. Consulta Datos de Productos. [online] Available at: <http://permisosfuncionamiento.controlsanitario.gob.ec/consulta/index.php> [Accessed 18 May 2021].
13.- Zahavi, D. and Weiner, L., 2020. Monoclonal Antibodies in Cancer Therapy. Antibodies, 9(3), p.34.
14.- Cho, H., Lee, S., Sim, S., Park, I., Lee, K., Kwak, M. and Kim, H., 2020. Cumulative incidence of chemotherapy-induced cardiotoxicity during a 2-year follow-up period in breast cancer patients. Breast Cancer Research and Treatment, 182(2), pp.333-343..
15.- Gong, I., Yan, A., Earle, C., Trudeau, M., Eisen, A. and Chan, K., 2020. Comparison of outcomes in a population-based cohort of metastatic breast cancer patients receiving anti-HER2 therapy with clinical trial outcomes. Breast Cancer Research and Treatment, 181(1), pp.155-165.


Lo sentimos, el formulario de comentarios está cerrado en este momento.