Eficacia de trabectedina en cáncer de ovario
El cáncer de ovario es una de las neoplasias ginecológicas malignas más frecuentes y la quinta causa más frecuente de muerte por cáncer en mujeres. Aproximadamente el 75% de las pacientes con cáncer de ovario presentan un estadio avanzado de la enfermedad asociado con un mal pronóstico, y la mayoría de los casos (> 80%) ocurren en mujeres mayores de 50 años. El tratamiento estándar de primera línea para la enfermedad avanzada consiste en citorreducción quirúrgica seguida de quimioterapia basada en platino / taxanos. A pesar de los avances logrados en los últimos años con cirugía y la introducción de nuevas opciones farmacológicas, como bevacizumab (primer antiangiogénico) en 2011 y olaparib (primer inhibidor de PARP) en 2014, alrededor del 70% -80% de las pacientes con cáncer epitelial recaen en los 2 años posteriores al diagnóstico. Actualmente, es un gran desafío clínico de la comunidad científica mejorar el pronóstico y calidad de vida de estas pacientes, particularmente encontrando las combinaciones correctas y la secuencia de uso de los tratamientos disponibles junto con la identificación de nuevas opciones de tratamiento.1
La trabectedina es un fármaco semisintético originalmente aislado de la ascidia Ecteinascidia turbinata; posee múltiples mecanismos de acción; además de actuar como un agente de unión al ADN, también inhibe la proliferación celular, lo que enconsecuencia, activa la apoptosis; tiene efectos antiinflamatorios e inmunomoduladores selectivos sobre el microambiente tumoral. Estos efectos se relacionan directamente con la inhibición de factores que promueven el crecimiento tumoral, metástasis y angiogénesis. Desde 2009, la trabectedina en combinación con doxorrubicina liposomal pegilada (DLP) ha sido aprobada en la Unión Europea y en aproximadamente otros 70 países alrededor del mundo para el tratamiento de pacientes con cáncer de ovario recurrente (COR) sensibles al platino.1
Esta aprobación se basó en los resultados del estudio aleatorizado de fase III OVA-301.1 Este ensayo fase 3 aleatorizado, multicéntrico y abierto tuvo como finalidad comparar la combinación de DLP y trabectedina con DLP solo en pacientes con COR avanzado. El objetivo del estudio fue identificar una combinación segura y eficaz que no contenga platino o taxanos para tratar el COR. Los principales criterios de inclusión fueron: pacientes con cáncer epitelial de ovario, trompas de Falopio o peritoneal primario medible que habían recibido un régimen previo que contenía platino; se clasificaron como no refractarios, no eran elegibles o no estaban dispuestos a recibir un nuevo tratamiento con terapia a base de platino.2
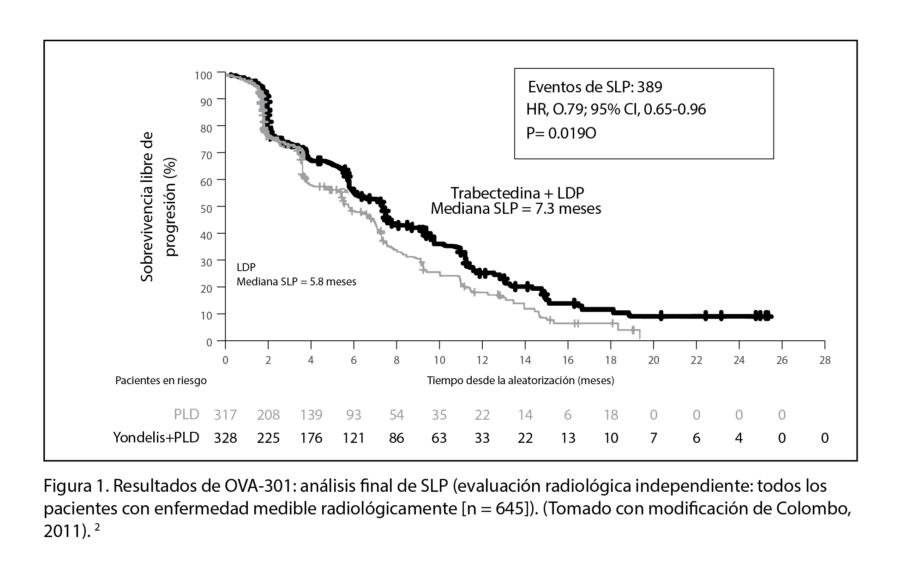
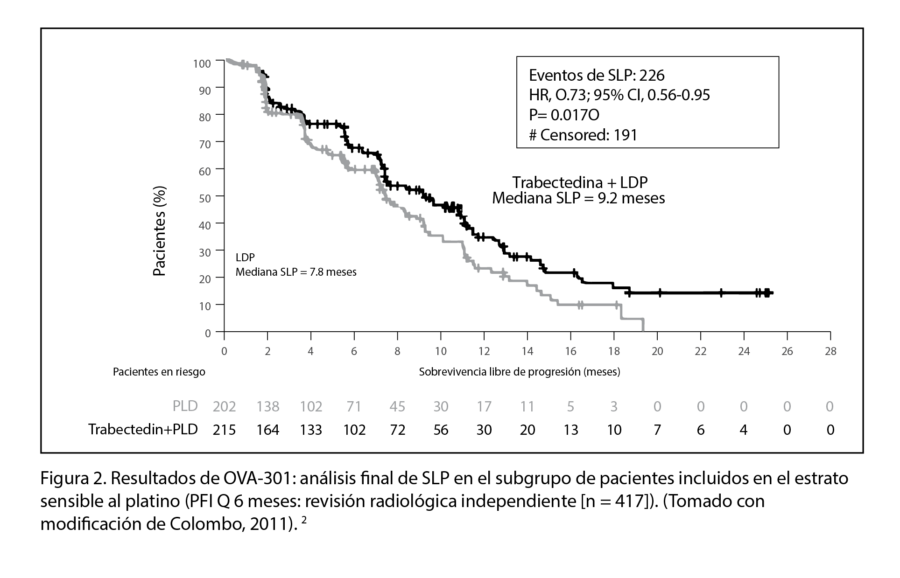
El ensayo alcanzó el criterio de valoración principal, el cual fue la supervivencia libre de progresión (SLP) según lo determinado por un comité de radiología independiente y un comité de oncología (Figura 1). En la evaluación del comité de revisión de radiología independiente, la combinación de trabectedina y DLP tuvo una ventaja estadísticamente significativa en la mediana de SLP en comparación con DLP solo (7,3 frente a 5,8 meses; cociente de riesgo [HR], 0,79; IC del 95%, 0,65 y 0,96). Es importante señalar que se lograron resultados similares cuando el comité de oncología de revisión independiente realizó una evaluación tanto radiológica como clínica de los pacientes (población por intención de tratar).1 En la población sensible al platino, OVA-301 demostró que la trabectedina más DLP mejora significativamente la SLP en comparación con DLP sola (mediana de SLP: 9,2 frente a 7,5 meses; cociente de riesgo [HR], 0,73; intervalo de confianza del 95% [IC], 0.56-0.95; p = 0.0170) cuando se administra después del fracaso de la quimioterapia de primera línea basada en platino (Figura 2).1-2
Se observó una actividad mejorada de trabectedina más DLP en pacientes con enfermedad parcialmente sensible al platino, con un intervalo libre de tratamiento de platino (TFIp) de 6 a 12 meses, quienes también obtuvieron una supervivencia global (SG) significativamente mayor con la combinación en comparación con DLP sola (mediana de SG, 22,4 frente a 16,4 meses; HR, 0,64; IC del 95%, 0,47–0,86; p = 0,0027). Además, un análisis exploratorio de los resultados de OVA-301 informó que los pacientes sensibles al platino con mutaciones BRCA1 podrían ser particularmente sensibles a la trabectedina más DLP, ya que obtuvieron una mediana de SLP notablemente más prolongada (13,6 frente a 5,5 meses, p = 0,0001) y SG (27,4 frente a 18,7 meses, p = 0,0093) que los tratados con DLP solo. De acuerdo con este análisis de OVA-301, el análisis preespecificado de otro estudio de fase III (OVC-3006), que comparó trabectedina más DLP versus DLP solo en el contexto de tercera línea en pacientes con COR sensible al platino, también informó una ventaja significativa de supervivencia entre portadores de la mutación BRCA1 / 2 (mediana de SG, 34,2 frente a 20,9 meses; HR, 0,54; IC del 95%, 0,33 a 0,90; p = 0,016) y una tendencia a mejorar la supervivencia entre los pacientes con un TFIp de 6 a 12 meses (24,8 frente a 17,4 meses; HR, 0,69; IC del 95%, 0,48-1,01; p = 0,056).1-2
El primer estudio prospectivo, real, paneuropeo, no intervencionista denominado NIMES-ROC (ClinicalTrials.gov Identifier: NCT02825420) fue diseñado con la finalidad de evaluar el uso de trabectedina más DLP en pacientes con ROC sensible al platino, y su eficacia y seguridad en la práctica clínica habitual en cinco países europeos.1
Los participantes elegibles incluyeron adultos con COR sensible al platino (COR-SP) que habían recibido uno o más ciclos de trabectedina / DLP antes de la inclusión de acuerdo con la autorización de comercialización. El 72,5% (218) de los pacientes fueron pretratados con al menos dos líneas de quimioterapia previas y recibieron una mediana de seis ciclos de trabectedina / DLP (rango: 1–24). La mediana de SLP fue de 9,46 meses (intervalo de confianza [IC] del 95%, 7,9-10,9) y la mediana de SG fue de 23,56 meses (IC del 95%, 18,1-34,1). Los pacientes que no recibieron tratamiento previo con un fármaco antiangiogénico obtuvieron una mediana de SLP mayor (p <0,007 y SG (p <0,048). Veinticuatro pacientes (11,0%) tuvieron una respuesta completa y 57 pacientes (26,1%) lograron una respuesta parcial para una tasa de respuesta objetiva (TRO) del 37,2%. Cincuenta y nueve pacientes (27,1%) tuvieron estabilización de la enfermedad para una tasa de control de la enfermedad del 64,2%. No se observaron diferencias estadísticamente significativas de la SLP, la SG o la TRO en relación con el estatus de BRCA1 / 2 y la sensibilidad al platino (Figura 3). Los eventos adversos (EA) de grado 3/4 más comunes fueron neutropenia (30,3%), anemia (6,4%), trombocitopenia (5,5%) y astenia (5,0%). No se produjeron muertes atribuidas a acontecimientos adversos relacionados con el tratamiento o acontecimientos adversos inesperados.1
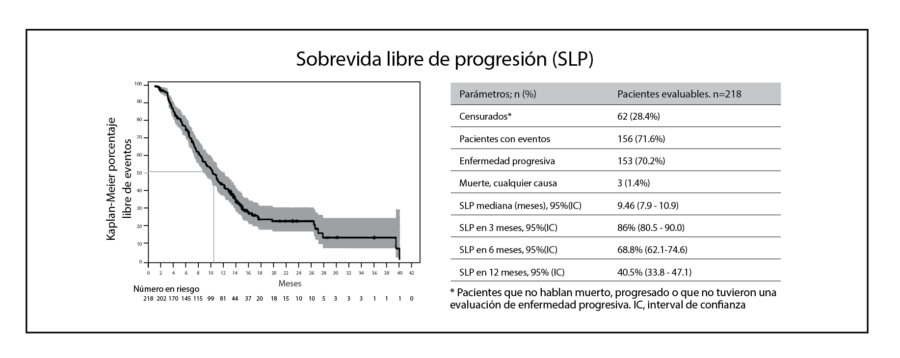
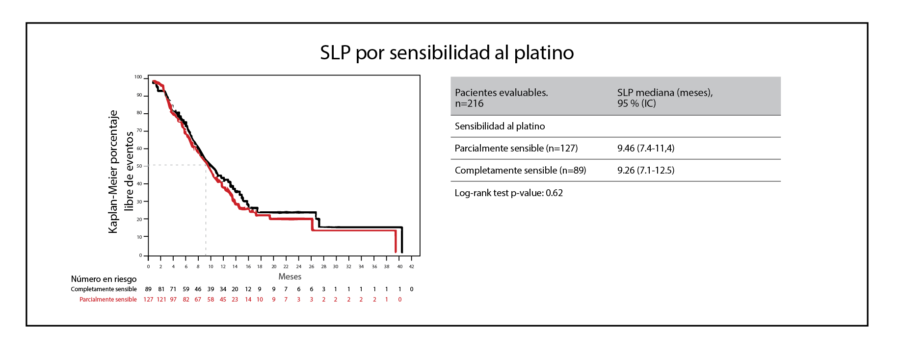
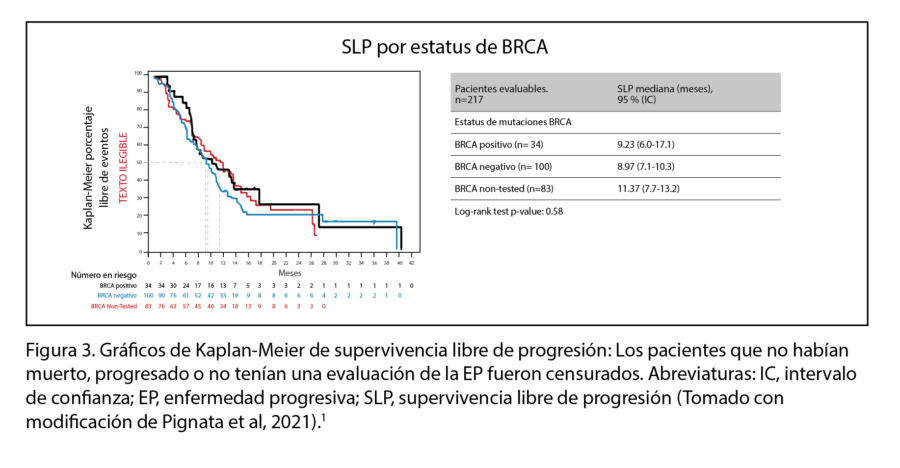
Sobre la base de estos resultados, se concluyó que la combinación de trabectedina / DLP representa una opción clínicamente significativa y segura para los pacientes con COR-SP independientemente del tratamiento previo con un fármaco antiangiogénico, siendo comparable con los resultados previamente observados en pacientes seleccionados y menos pretratados de ensayos clínicos.1
Referencias:
- Pignata S, Scambia G, Villanucci A, Naglieri E, Ibarbia MA, Brusa F, Bourgeois H, Sorio R, Casado A, Reichert D, Dopchie C, De Rivas B, de Sande LM. A European, Observational, Prospective Trial of Trabectedin Plus Pegylated Liposomal Doxorubicin in Patients with Platinum-Sensitive Ovarian Cancer. Oncologist. 2021 Apr;26(4):e658-e668. doi: 10.1002/onco.13630. Epub 2021 Jan 3. PMID: 33289956; PMCID: PMC8018301.
- Colombo N. Efficacy of trabectedin in platinum-sensitive-relapsed ovarian cancer: new data from the randomized OVA-301 study. Int J Gynecol Cancer. 2011 May;21 Suppl 1:S12-6. doi: 10.1097/IGC.0b013e318217b321. PMID: 21540666.

Lo sentimos, el formulario de comentarios está cerrado en este momento.