
RAMUCIRUMAB LA ALTERNATIVA EN SEGUNDA LÍNEA PARA PACIENTES CON CÁNCER GÁSTRICO EVIDENCIA CLÍNICA Y DE MUNDO REAL
El cáncer de pulmón es la principal causa de incidencia de cáncer y mortalidad relacionada con el cáncer en todo el mundo; con supervivencia promedio a los 5 años del 15 % en los EE. UU. El cáncer de pulmón de células no pequeñas (NSCLC) representa aproximadamente el 85 % de todos los casos de cáncer de pulmón y aproximadamente el 70 % de los pacientes con NSCLC tienen enfermedad metastásica o localmente avanzada en el momento del diagnóstico. Para los pacientes con enfermedad metastásica o localmente avanzada y una mutación accionable (EGFR, ALK, ROS1, BRAF y NTRK), la terapia dirigida es el tratamiento de referencia actual; sin embargo, un número significativo de pacientes carece de una mutación accionable. La quimioterapia en forma de doblete de platino solía ser el tratamiento estándar de atención para estos pacientes, siendo docetaxel una de las opciones de tratamiento de segunda línea. La quimioterapia de segunda línea se asoció con una tasa de respuesta deficiente (<10 %) y una mediana de supervivencia de 8 meses como máximo. En 2015, la FDA aprobó nivolumab en base a dos grandes ensayos aleatorizados de fase III que mostraron una supervivencia global (SG) más prolongada con nivolumab que con docetaxel.1

Desde la aprobación de nivolumab, otros dos inhibidores de puntos de control del ciclo celular también fueron aprobados en entornos de segunda línea para pacientes con NSCLC avanzado o metastásico [atezolizumab y pembrolizumab (para PD-L1≥1 %)]. Con la llegada de la inmunoterapia, se pensó que ya no se utilizaría el régimen de tratamiento basado en docetaxel. Recientemente, el doblete de pembrolizumab más platino se convirtió en la opción de tratamiento preferida para los pacientes que no tienen una mutación conductora procesable, según los datos de dos estudios emblemáticos como lo son KEYNOTE-189 y KEYNOTE-407. El beneficio de supervivencia con quimioterapia más inmunoterapia se observó independientemente de expresión de PD-L1. La monoterapia con pembrolizumab es una opción para aquellos con una expresión alta de PD-L1 de ≥50 %. Esto se basa en el estudio KEYNOTE-024 que mostró un beneficio de supervivencia significativo con pembrolizumab en comparación con el doblete de platino estándar. El doblete de platino más atezolizumab y bevacizumab es otra opción de tratamiento preferida para estos subgrupos de pacientes, según datos recientes del ensayo IMPOWER 150 que demostró beneficio en supervivencia .
Entre el 40 % al 50 % de los pacientes no responderán a la combinación de quimioinmunoterapia y la mayoría de ellos progresarán en el futuro, por lo que necesitarán un tratamiento de segunda línea. Por lo tanto, existe una necesidad sustancial de opciones de tratamiento de segunda línea en pacientes con NSCLC avanzado. Es aquí donde el papel de papel de ramucirumab en pacientes con NSCLC se estudió en primera instancia logrando posicionarse luego en primera línea.1
La angiogénesis es un paso importante en la proliferación y el crecimiento del cáncer. VEGF es uno de los factores más importantes asociados con la angiogénesis; su inhibición puede suprimir el crecimiento tumoral. Ramucirumab es un anticuerpo monoclonal recombinante de la clase de inmunoglobulina G1 que se dirige al dominio extracelular de VEGFR-2. VEGFR-2 se regula significativamente en la vasculatura tumoral en la mayoría de los tumores sólidos. Al bloquear VEGFR-2, ramucirumab previene la angiogénesis y el crecimiento tumoral; 1

El estudio REVEL fue un estudio de fase III, multicéntrico, aleatorizado, doble ciego, controlado con placebo que incluyó a pacientes con NSCLC en estadio IV patológicamente confirmado que habían progresado durante o después de la quimioterapia basada en platino, con o sin bevacizumab. Un total de 1253 pacientes fue aleatorizado en proporción de 1:1 para recibir docetaxel con placebo (n=628) ó docetaxel con ramucirumab (n=625) cada 3 semanas. El ORR fue del 14 % frente al 23 % (OR 1,89, IC del 95 % 1,41–2,54, p<0,0001), la mediana de PFS fue de 3,0 meses frente a 4,5 meses (HR 0,76, IC del 95 % 0,68–0,86) y la mediana de OS fue de 9,1 meses vs 10,5 meses (HR 0,86, IC 95% 0,75-0,98) en el grupo placebo y ramucirumab respectivamente. La mayoría de los subgrupos tuvo mejor supervivencia con ramucirumab, aunque el estudio no tuvo la potencia necesaria para el análisis de subgrupos; a destacar que no hubo un beneficio evidente de ramucirumab en pacientes de edad avanzada. El setenta y nueve por ciento de los pacientes en el brazo de ramucirumab y el 71 % de los pacientes en el brazo sin ramucirumab experimentaron eventos adversos relacionados con el tratamiento de grado ≥3. El treinta y siete por ciento de los pacientes (n=231) en el grupo de ramucirumab tuvo neutropenia de grado 4 en comparación con el 28 % en el grupo sin ramucirumab; , los pacientes en el brazo de ramucirumab tenían más sangrado, fatiga, estomatitis, inflamación de la mucosa y disgeusia. No hubo diferencia en los eventos de sangrado gastrointestinal y del tracto respiratorio entre los dos grupos. En base a una mejora en la supervivencia con una ganancia neta de 1,4 meses, la FDA aprobó el uso de ramucirumab junto con docetaxel para pacientes con NSCLC metastásico con progresión de la enfermedad durante o después de la quimioterapia doble con platino, el 12 de diciembre de 2014.1
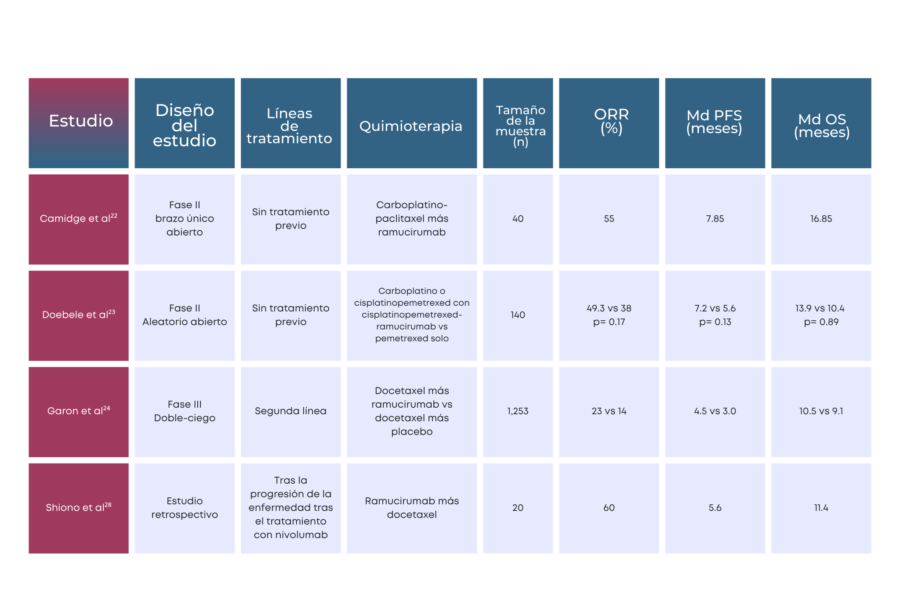
Dos ensayos aleatorizados han evaluado ramucirumab en pacientes con NSCLC avanzado o metastásico en primera línea; el primero de ellos fue un estudio de fase II, multicéntrico, abierto, de un solo brazo, en el cual se inscribieron 40 pacientes con NSCLC en estadio IIIB o IV confirmado histológicamente, cada uno de estos pacientes recibió ramucirumab a la dosis de 10 mg/kg por infusión intravenosa además del doblete de platino estándar (carboplatino-paclitaxel) cada 3 semanas. El tratamiento continuó hasta por seis ciclos o hasta que hubo evidencia de progresión de la enfermedad o toxicidad intolerable; la tasa de respuesta global (ORR) fue del 55 %, incluido el 52,5 % (n=21) respuesta parcial, el 35,0 % (n=14) enfermedad estable y sólo un paciente logró una respuesta completa; la mediana de supervivencia libre de progresión (PFS) fue de 7,85 meses y la mediana de sobrevivencia global (OS) fue de 16,85 meses. El ochenta y cinco por ciento de los pacientes (n=35) experimentaron efectos adversos relacionados con el tratamiento , la mayoría grado 2 o 3 dentro de los más comunes fatiga, neuropatía periférica, náuseas, epistaxis y mialgia. Es de destacar que no se informó hemoptisis de grado ≥3 en este estudio.
El estudio de Doebele et al. fue un estudio de fase II, aleatorizado, abierto y multicéntrico en el que participaron 140 pacientes con NSCLC en estadio IV confirmado histológicamente; la aleatorización fue 1:1 en adenocarcinoma para recibir un doblete de platino (pemetrexed más carboplatino o cisplatino) ó un doblete de platino con ramucirumab cada 3 semanas durante un máximo de 4 a 6 ciclos, la terapia de mantenimiento incluyó pemetrexed con o sin ramucirumab. Los pacientes con NSCLC escamoso recibieron gemcitabina en lugar de pemetrexed y la mitad de los pacientes recibieron ramucirumab de mantenimiento. La ORR, la PFS y la OS no fueron significativamente diferentes entre los dos brazos: la ORR fue del 49,3 % frente al 38,0 % (p=0,1797), la mediana de la PFS fue de 7,2 frente a 5,6 meses (p=0,1318), la mediana de la OS fue de 13,9 frente a 10,4 meses (p=0,8916) en el brazo ramucirumab y no ramucirumab respectivamente. Sobre la base de estos resultados, no se considera a Ramucirumab como un estándar de atención en el entorno de primera línea en el tratamiento de NSCLC avanzado o metastásico.1

Los hallazgos de los tres ensayos mencionados anteriormente se resumen en la Tabla 1. Docetaxel en combinación con nintedanib (especialmente en pacientes con adenocarcinoma) o paclitaxel en combinación con bevacizumab también podrían ser opciones terapéuticas potenciales, especialmente después de la progresión de la enfermedad en el tratamiento combinado de quimio-inmunoterapia. A su vez Ramucirumab más docetaxel ha mostrado una buena tasa de respuesta cuando se administra tras el fracaso de nivolumab.1
En resumen, ramucirumab en combinación con docetaxel es una opción para pacientes con NSCLC metastásico que han progresado con quimioterapia con platino. La combinación confiere 1,4 meses de mejora en la mediana de supervivencia. Dado que la ganancia de supervivencia es modesta, la adición de ramucirumab debe individualizarse para pacientes más jóvenes con un buen estado funcional.1
En el NSCLC metastásico con mutación de EGFR, los resultados de los inhibidores de la tirosina quinasa de EGFR difieren históricamente según el tipo de mutación presente, con un beneficio menor informado en pacientes con mutaciones ex21L858R versus ex19del. Las mutaciones activadoras de EGFR son consideradas un factor predictivo importante para la respuesta a las terapias con inhibidores de la tirosina quinasa (TKI) de EGFR ; sin embargo, el grado de beneficio puede diferir según el tipo de mutación de EGFR, que ha demostrado ser un marcador de pronóstico independiente.2
Sobre la base de estos antecedentes se investigó si los subtipos de mutaciones activadoras de EGFR afectan los resultados del tratamiento en el estudio de fase III RELAY. También se exploraron las asociaciones entre el tipo de mutación de EGFR y las alteraciones genéticas coexistentes preexistentes y emergentes del tratamiento.2
Los pacientes con NSCLC metastásico, una mutación EGFR ex19del o ex21L858R y sin metástasis en el sistema nervioso central fueron aleatorizados (1:1) para recibir erlotinib (150 mg/día) con ramucirumab (10 mg/kg; RAMþERL) o placebo (PBOþERL), cada 2 semanas, hasta progresión definida RECIST v1.1 o toxicidad inaceptable. El criterio principal de valoración fue la supervivencia libre de progresión (PFS). Los criterios de valoración secundarios y exploratorios incluyeron la tasa de respuesta global (ORR), la duración de la respuesta (DOR), la PFS2, el tiempo hasta la quimioterapia (TTCT), la seguridad y los análisis de secuenciación de próxima generación.2
Los pacientes con mutaciones ex19del y ex21L858R tenían características clínicas y perfiles de comportamiento similares; las tasas de PFS a un año para los pacientes con ex19del fueron del 74 % para RAMþERL frente al 54 % para PBOþERL; (Figura 2.A) para ex21L858R las tasas fueron del 70 % (RAMþERL) frente al 47 % (PBOþERL) (Figura 2.B). Se observaron beneficios de tratamiento similares (ORR, DOR, PFS2 y TTCT) en pacientes tratados con RAMþERL con ex19del y ex21L858R. La conmutación inicial de TP53 se asoció con resultados superiores para RAMþERL en los subgrupos ex19del y ex21L858R. La tasa de mutación de EGFR T790M en la progresión fue similar entre los brazos de tratamiento y por tipo de mutación.2
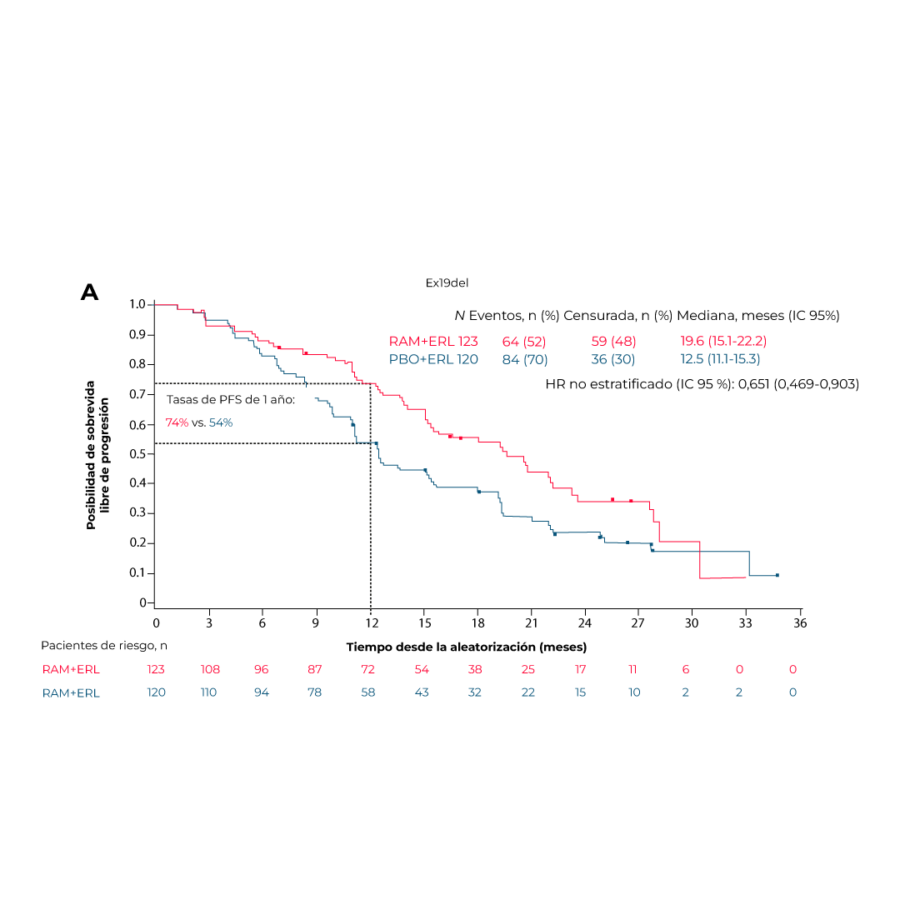
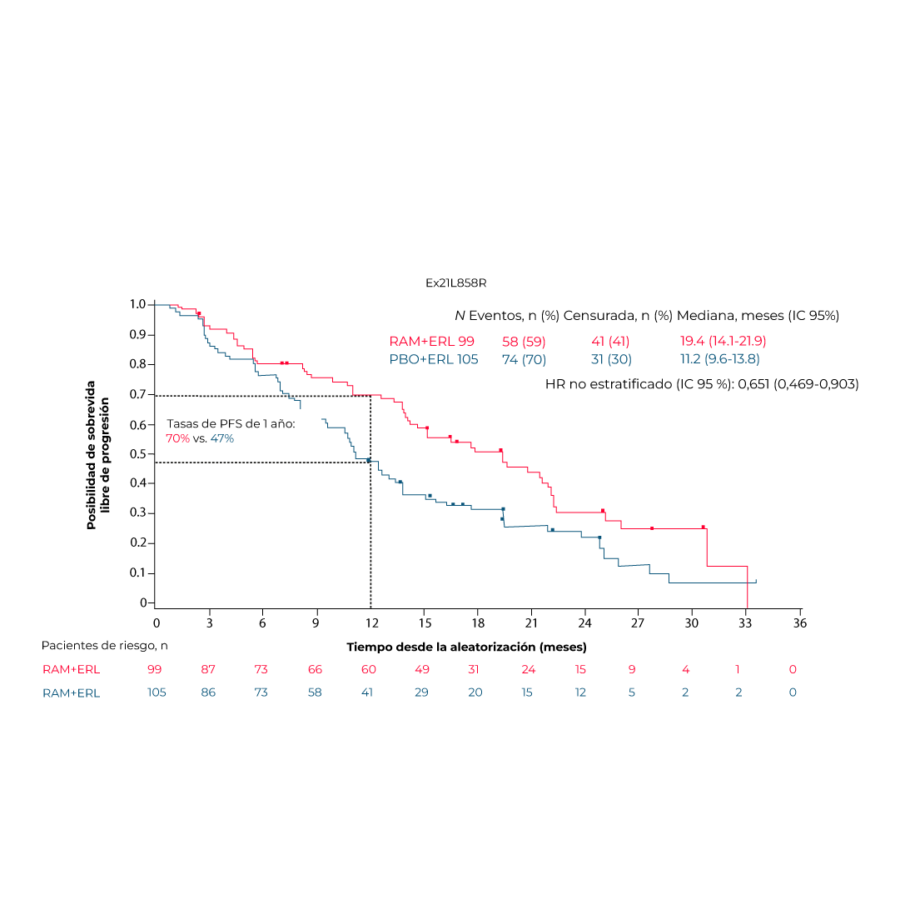
Se puede concluir que el estudio RELAY demuestra que RAMþERL tiene un beneficio clínico significativo tanto para el NSCLC EGFR ex19del como para el ex21L858R, lo que respalda que este régimen sea adecuado para pacientes con cualquiera de estos tipos de mutación EGFR. Sin embargo, dado que los pacientes con ex21L858R positivo históricamente tienen peores resultados en relación con ex19del en respuesta a las monoterapias con EGFR-TKI, este subgrupo de NSCLC con mutación de EGFR puede tener mayor prioridad para agregar un antiangiogénico a un EGFR-TKI. Estos hallazgos proporcionan evidencia de que los pacientes con mutaciones EGFR ex19del y ex21L8585R no tienen una respuesta heterogénea a la terapia dirigida EGFR-TKI cuando se combinan con ramucirumab. La evidencia clínica descrita puede ayudar a los médicos a proporcionar una estrategia de tratamiento personalizada y permitir que las decisiones de tratamiento se tomen de manera más racional.2
Sobre la base de los resultados del estuido RELAY, Ramucirumab fue aprobado por la FDA en combinación con erlotinib para el tratamiento de primera línea del cáncer de pulmón de células no pequeñas metastásico con deleciones del exón 19 del receptor del factor de crecimiento epidérmico o mutaciones del exón 21 (L858R).3
Referencias:
- Uprety D. Clinical utility of ramucirumab in non-small-cell lung cancer. Biologics: Targets & Therapy. 2019;13:133.
- Nakagawa K, Nadal E, Garon EB, Nishio M, Seto T, Yamamoto N, Park K, Shih JY, Paz-Ares L, Frimodt-Moller B, Zimmermann AH. RELAY Subgroup Analyses by EGFR Ex19del and Ex21L858R Mutations for Ramucirumab Plus Erlotinib in Metastatic Non–Small Cell Lung Cancer. Clinical Cancer Research. 2021 Oct 1;27(19):5258-71.
- Cancerletter. Disponible en: www.cancerletter.com. Jun 5, 2020. Consultado el 24 de agosto del 2022.

Lo sentimos, el formulario de comentarios está cerrado en este momento.