ESPONDILITIS ANQUILOSANTE
La espondilitis anquilosante (EA) es una enfermedad inflamatoria reumática crónica que afecta a entre el 0,1% y el 0,5% de la población global.1,2 En Latinoamérica se estiman 10,2 casos por cada 10.000 habitantes.2
La espondilitis anquilosante (EA) representa el principal subtipo de las espondiloartritis (EspA), e involucra frecuentemente al esqueleto axial (cabeza, cuello, columna, tórax y pelvis), las articulaciones periféricas y las entesis (inserciones de los tendones y ligamentos en el hueso), conduciendo a un deterioro funcional de los pacientes y a una disminución en la calidad de vida 1-3 Es más frecuente en hombres que en mujeres, con una relación de 2-3:1, la edad de inicio es menor de los 45 años; su clínica está determinada por la reacción autoinmune que inicia en la región axial causando la fusión de cuerpos vertebrales por la formación de puentes óseos entre vértebras.4
Características Clínicas de la Espondilitis Anquilosante



En el Ecuador no se cuenta con datos epidemiológicos actualizados sobre espondilitis anquilosante (EA); sin embargo, en un estudio recientemente realizado en la Unidad Técnica de Reumatología del Hospital de Especialidades Carlos Andrade Marín (HECAM) que incluyó un total de 120 pacientes, se obtuvieron los siguientes resultados:4
Características de los pacientes con EA del HECAM (año-2020)

INACTIVANDO LA ESPONDILITIS ANQUILOSANTE
De acuerdo con el ACR-SAA-SPARTAN 2019 (American College of Rheumatology / Spondylitis Association of America / Spondyloarthritis Research and Treatment Network) los pacientes adultos con espondilitis anquilosante (EA) y espondiloartritis axial (EsA) de tipo radiográfica activa pueden recibir tratamiento continuo con fármacos antiinflamatorios no esteroideos (AINEs); mientras, que los pacientes con enfermedad estable pueden recibirlos a demanda.1,6 No obstante, existen controversias con respecto al papel de los AINEs en la prevención de la progresión radiográfica de la enfermedad.6
Tras la aprobación del primer inhibidor del factor de necrosis tumoral alfa (anti-TNFα) para su uso en la espondilitis anquilosante (EA) hace 17 años; el tratamiento con anti-TNFα se ha convertido en la terapia principal para la EA activa, debido a su alta tasa de respuesta, además de lograr el control de la inflamación axial, junto con el amplio espectro de manifestaciones extra-axiales en la piel, las articulaciones periféricas, las entesis, los tendones, los ojos y el intestino.3,6 Hasta la fecha los anti-TNFα más estudiados en el tratamiento de la EA son: adalimumab, etanercept, golimumab e infliximab.7
Mediante estudios clínicos controlados aleatorizados se ha demostrado que hasta un 30% de los pacientes con espondiloartritis axial (EsA) o EA pueden alcanzar la inactividad de la enfermedad, definida como un índice de actividad ASDAS (Ankylosing Spondylitis Disease Activity Score) por debajo de 1.3 a las 24 semanas de inicio del tratamiento con anti-TNFα.8,9 Por lo tanto, el ACR-SAA-SPARTAN 2019 incluye en sus recomendaciones el tratamiento con anti-TNFα en adultos con EA activa a pesar del uso AINEs.1
El abordaje no farmacológico juega un rol importante en el manejo de los pacientes; las Guías ASAS-EULAR 2016 (The Assessment of Spondylarthritis International Society and European League Against Rheumatism) recomiendan considerar la fisioterapia, que se eduque a los pacientes sobre la enfermedad y que se les anime a hacer ejercicio de forma regular y a dejar de fumar. La inclusión de los ejercicios aeróbicos, cardiorrespiratorios y los programas educativos puede conducir a mejores resultados clínicos.6
Objetivos del tratamiento



ADALIMUMAB EN EL TRATAMIENTO DE LA ESPODILITIS ANQUILOSANTE
El adalimumab es un anticuerpo monoclonal compuesto por la inmunoglobulina G1-κ bivalente, con alta afinidad, completamente humano, que se dirige específicamente al TNF soluble y unido a la membrana.10 A través de los estudios clínicos pivotales se ha demostrado su eficacia y seguridad en el tratamiento de los pacientes con espondilitis anquilosante (EA), por lo que cuenta con aprobación para su tratamiento por parte de la FDA (Food and Drug Administration) y de la EMA (European Medicines Agency) desde 2006.10-12
Adicionalmente, adalimumab cuenta con aprobación por parte de la FDA y de la EMA para las siguientes indicaciones.13,14



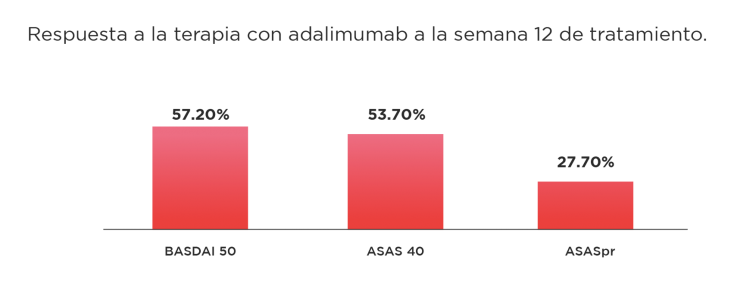
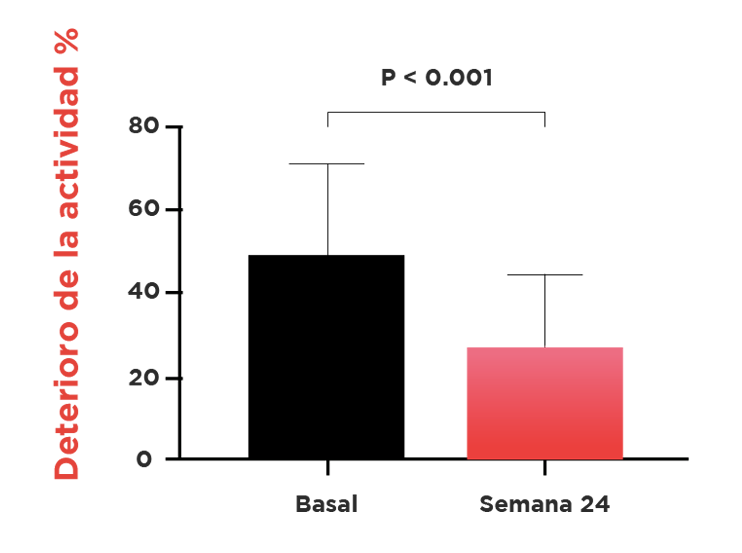
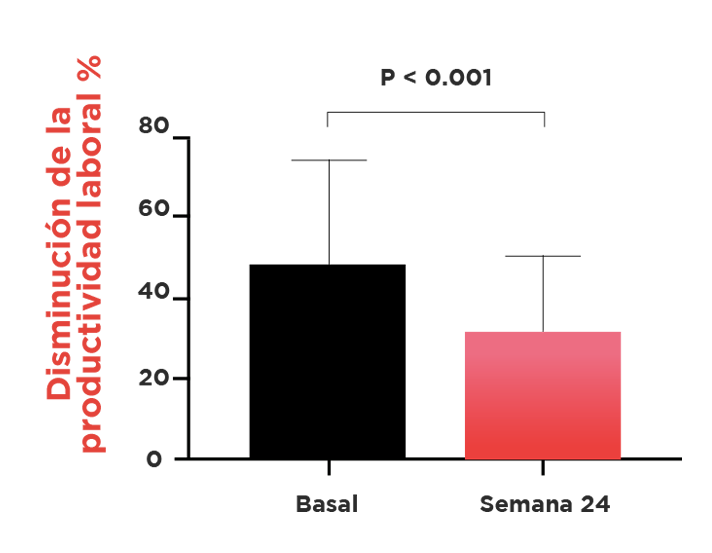
La respuesta al tratamiento se evaluó mediante el índice de actividad BASDAI (Bath Ankylosing Spondylitis Disease Activity Index); Grupo ASAS (Assessment in SpondyloArthritis International Society); ASASpr (Remisión Parcial).

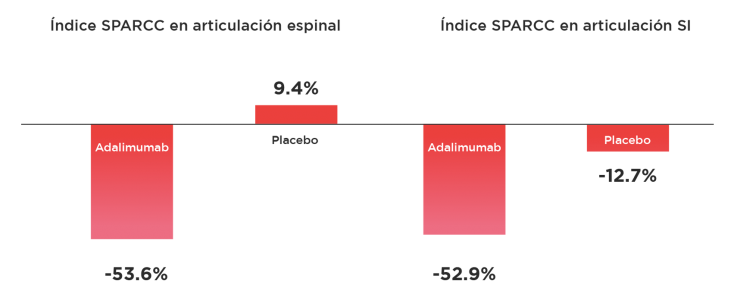
La inflamación de la articulación espinal y sacroilíaca (SI), se evaluó mediante el índice de resonancia magnética (IRM) SPARCC (Spondyloarthritis Research Consortium of Canada)


Referencias:
1. Ward, M., Deodhar, A., Gensler, L. el al. 2019 Update of the American College of Rheumatology/Spondylitis Association of America/Spondyloarthritis Research and Treatment Network Recommendations for the Treatment of Ankylosing Spondylitis and Nonradiographic Axial Spondyloarthritis. Arthritis Care Res (Hoboken). 2019 Oct;71(10):1285-1299. doi: 10.1002/acr.24025. Epub 2019 Aug 21. PMID: 31436026; PMCID: PMC6764857.
2. Macfarlane, T., Abbood, H., Pathan, E. et al.Relationship between diet and ankylosing spondylitis: A systematic review. Eur J Rheumatol. 2018 Mar;5(1):45-52. doi: 10.5152/eurjrheum.2017.16103. Epub 2017 Oct 25. PMID: 29657875; PMCID: PMC5895151.
3. Mounach, A., El Maghraoui, A. Efficacy and safety of adalimumab in ankylosing spondylitis. Open Access Rheumatol. 2014 Aug 13;6:83-90. doi: 10.2147/OARRR.S44550. PMID: 27790037; PMCID: PMC5045114.
4. Manotoa, M., Armijos, M. Evaluar la calidad de vida y funcionalidad en pacientes con espondilitis anquilosante. Revista Médica Científica CAMbios. 2020;19(1). DOI: https://doi.org/10.36015/cambios.v19.n1.2020.475
5. Bruner, V., Atteno, M., Spanò, A. et al. Biological therapies for spondyloarthritis. Ther Adv Musculoskelet Dis. 2014 Jun;6(3):92-101. doi: 10.1177/1759720X14535512. PMID: 24891880; PMCID: PMC4040940.
6. Agrawal, P., Machado, P. Recent advances in managing axial spondyloarthritis. F1000Res. 2020 Jul 13;9:F1000 Faculty Rev-697. doi: 10.12688/f1000research.22577.1. PMID: 32704350; PMCID: PMC7359748.
7. Maxwell, L., Zochling, J., Boonen, A. et al.TNF-alpha inhibitors for ankylosing spondylitis. Cochrane Database of Systematic Reviews 2015, Issue 4. Art. No.: CD005468.DOI: 10.1002/14651858.CD005468.pub2.
8. Lindström, U., Olofsson, T., Wedrén, S. et al. Biological treatment of ankylosing spondylitis: a nationwide study of treatment trajectories on a patient level in clinical practice. Arthritis Res Ther. 2019 May 28;21(1):128. doi: 10.1186/s13075-019-1908-9. PMID: 31138285; PMCID: PMC6540538.
9. Navarro-Compán,V., Otón, T., Loza, E. et al. Consenso ASAS en nomenclatura en español para las espondiloartritiss. Reumatol Clin. 2020 Sep-Oct;16(5 Pt 1):333-338. English, Spanish. doi: 10.1016/j.reuma.2018.07.014. Epub 2018 Sep 5. PMID: 30193774.
10. Kapoor, S., Kaushik, V., Jain, R. et al. Real-life Tolerability and Effectiveness of Adalimumab Biosimilar in Ankylosing Spondylitis: the Adalimumab Biosimilar Patient Registry Data. ACR Open Rheumatol. 2019 Aug 12;1(8):480-484. doi: 10.1002/acr2.11067. PMID: 31777828; PMCID: PMC6857999.
11. Drugs.com |Humira (adalimumab) FDA Approval History. 2021. (Online). Consultado por última vez en junio de 2021. Disponible en: https://www.drugs.com/history/humira.html
12. European Medicines Agency | Humira: Procedural steps taken and scientific information after the authorization. 2021. (Online). Consultado por última vez en junio de 2021. Disponible en: https://www.ema.europa.eu/en/documents/procedural-steps-after/humira-epar-procedural-steps-taken-scientific-information-after-authorisation_en.pdf
13. Ellis CR, Azmat CE. Adalimumab. 2021 May 5. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2021 Jan–. PMID: 32491812.
14. European Medicines Agency | Humira (adalimumab): An overview of Humira and why it is authorised in the EU.2020. (Online). Consultado por última vez en junio de 2021. Disponible en: https://www.ema.europa.eu/en/documents/overview/humira-epar-medicine-overview_en.pdf
15. Tu, L., Xie, Y., Liao, Z. et al. Cost of Illness, Quality of Life, and Work Outcomes in Active Ankylosing Spondylitis Patients Treated With Adalimumab in China. Front Public Health. 2020 Nov 24;8:602334. doi: 10.3389/fpubh.2020.602334. PMID: 33330342; PMCID: PMC7732412.

Lo sentimos, el formulario de comentarios está cerrado en este momento.