
Simposio de Cáncer GÉNITO-URINARIO de la Sociedad Americana de Oncología (ASCO GU) HIGHLIGHTS
Uno de los eventos que concentra atención a nivel mundial en el área de tumores génito-urinarios es el Simposio organizado por la Sociedad Americana de Oncología; a este evento concurren urólogos, oncólogos y otras especialidades involucradas en el manejo multidisciplinario de esta patología. A continuación, mostramos algunas novedades exhibidas en la reunión virtual con centro en el cáncer de próstata.
Incremento de diagnóstico de cáncer metastásico relacionado a disminución de tamizaje.
Aun cuando el tamizaje con el uso de Antígeno Prostático Específico (PSA por sus siglas en inglés) mostró reducción en la mortalidad y la presencia de enfermedad metastásica, también se encontró un incremento en el sobrediagnóstico con implicaciones en calidad de vida1. Por lo anterior, el USPSTF (US Preventive Task Force) quitaron la recomendación de tamizaje entre los años 2008 a 2012. Por esta razón el equipo del Dr. Vidit Sharma buscó evaluar si hubo algún impacto de este cambio de conducta en el diagnóstico de enfermedad avanzada. Para ello se evaluaron los datos de la Asociación Norteamericana de Registros Centrales de Cáncer entre el año 2002 a 2016 en cada estado.
Desde el año 2008 hasta el año 2016 el porcentaje promedio de hombres tamizados disminuyó del 61.8% al 50.5%; mientras, la incidencia de enfermedad maligna metastásica de próstata en el diagnóstico se incrementó del 6.4 al 9.0 por 100 000 hombres con una diferencia estadísticamente significativa.
Esto muestra la necesidad del diálogo entre médicos y pacientes para sopesar los riesgos, pero el tamizaje es una herramienta que puede ser considerada en la práctica cotidiana2.
Equivalencia de hallazgos genéticos entre biopsia tisular y biopsia líquida.
La biopsia líquida se ha convertido en una herramienta práctica para definir la dinámica tumoral sobre el tiempo estudiando áreas como el genoma, epigenoma, transcriptoma y proteoma; contribuye con biomarcadores predictivos, pronósticos y de respuesta3.
Para determinar la validez clínica de la detección de alteraciones genómicas en plasma de pacientes con Cáncer de Próstata Resistente a la Castración metastásico, el grupo de Tukachinsky evaluó el plasma de 3 324 pacientes (incluyendo 1 674 pacientes del estudio TRITON 2/3 y 1 660 de evaluaciones rutinarias). Los resultados se compararon con el perfil genómico comprehensivo de 2 006 biopsias prostáticas de pacientes con cáncer de próstata metastásico. Se analizó concordancia entre 837 pacientes que tenían tanto biopsia tisular como líquida. El 94% tuvo ADN (ácido desoxirrubinucleico) circulante detectable; se encontraron mutaciones en los genes BRCA 1/2 en el 8.8% y en el análisis de concordancia se encontró que el 8.6% presentó dichas mutaciones en la biopsia tisular mientras que de ellos el 93% fue identificado en el ADN circulante y 20 pacientes presentaron la mutación en el ADN circulante pero no en la biopsia de tejido. Se detectaron adicionalmente reversiones subclonales BRCA 1/2, alteraciones del receptor androgénico, amplificaciones, así como alteración de varias vías implicadas en el cáncer. En este estudio se encuentra que la mayoría de los pacientes con cáncer de próstata avanzado (94%) tienen abundante ADN circulante4.
Dificultades en uso de tratamientos combinados para el manejo del Cáncer de Próstata Resistente a la Castración Metastásico.
Docetaxel es un medicamento que ha demostrado incremento en la Supervivencia Global en los pacientes con Cáncer de Próstata Resistente a la Castración Metastásico, se ha considerado como uno de los estándares de tratamiento para esta enfermedad5. Sin embargo, así como ha sido estudiada por largo tiempo su eficacia, así mismo se han evaluado varios mecanismos que pueden ocasionar resistencia a su uso en esta enfermedad6.
Se estudió la combinación de Saracatinib (inhibidor de la tirosina quinasa, oral altamente selectivo de los miembros de la familia Abl y Src), el estudio tuvo como base experiencia pre-clínica que mostró sinergia con docetaxel. Se enrolaron 10 pacientes en la fase I del estudio y 142 se aleatorizaron en la fase II (la aleatorización fue 1:1 de docetaxel y saracatinib versus docetaxel y placebo). Al comparar a los dos grupos en la fase II se encontró un HR de 1.35 (IC95% de 1.07 a 1.70) para la Supervivencia Libre de Progresión o lo que se traduce en un incremento del 37% en el riesgo de progresión con el uso de la combinación. El HR para Supervivencia Global fue de 1.42 o traducido en un incremento del 42% en el riesgo de Muerte. Finalmente, se encontró un incremento de la toxicidad en el tratamiento de combinación. En este caso y en esta combinación puntual no existe beneficio de añadir un tratamiento a Docetaxel. Futuros estudios con combinaciones distintas a saracatinib ampliarán o modificarán lo encontrado para el futuro7.
Comparación del uso de enzalutamida contra flutamida sumados a Terapia de Deprivación Androgénica para el manejo del Cáncer de Próstata Resistente a la Castración.
El uso de tratamientos contra el receptor de andrógenos de nueva generación ha mostrado en varios estudios beneficio clínico en comparación con los medicamentos de generación anterior (flutamida o bicalutamida); en este contexto se realizó el estudio fase IV AFTERCAB en Japón. Entre noviembre del 2016 a marzo del 2020 se evaluaron pacientes de dicho país con cáncer de próstata resistente a la castración metastásico o no metastásico. 206 pacientes fueron aleatorizados, la media de tiempo de exposición a tratamiento fue de 14.3 meses para enzalutamida y de 5.6 meses para flutamida; el tiempo inicial para la progresión fue mayor para enzalutamida con 21.4 meses versus 5.8 meses para flutamida, la disminución de riesgo de progresión fue del 58% (HR 0.42 con IC95% 0.29-0.61) y con diferencia significativa. Este estudio suma evidencia al concepto de superioridad de enzalutamida en comparación a tratamientos de generación previa como es flutamida en este caso para el manejo de los pacientes con cáncer de próstata resistente a la castración8.
Evaluación de la profundidad de respuesta por PSA respecto a Supervivencia Global y Supervivencia Libre de Metástasis en el Cáncer de Próstata Resistente a la Castración No Metastásico.
El uso de enzalutamida en el estudio PROSPER demostró incremento tanto en la Supervivencia Global como en la Supervivencia Libre de Metástasis. Y aunque el estudio PROSPER previamente fue presentado, es interesante el estudio detallado de las distintas variables relacionadas con eficacia o seguridad.
En el presente caso Hussain agrupó los distintos niveles de disminución de PSA y los relacionó con Supervivencia Global y Supervivencia Libre de Progresión.
En lo referente a Supervivencia Global se encuentra un incremento de esta, relacionada a una mayor disminución del valor inicial de PSA.
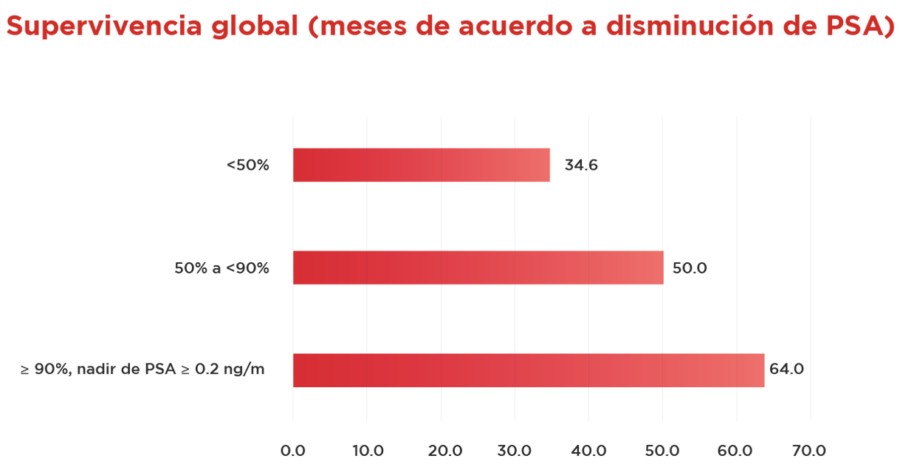
Se encuentra una importante disminución del riesgo relacionado con Supervivencia Global así como Supervivencia Libre de Metástasis.
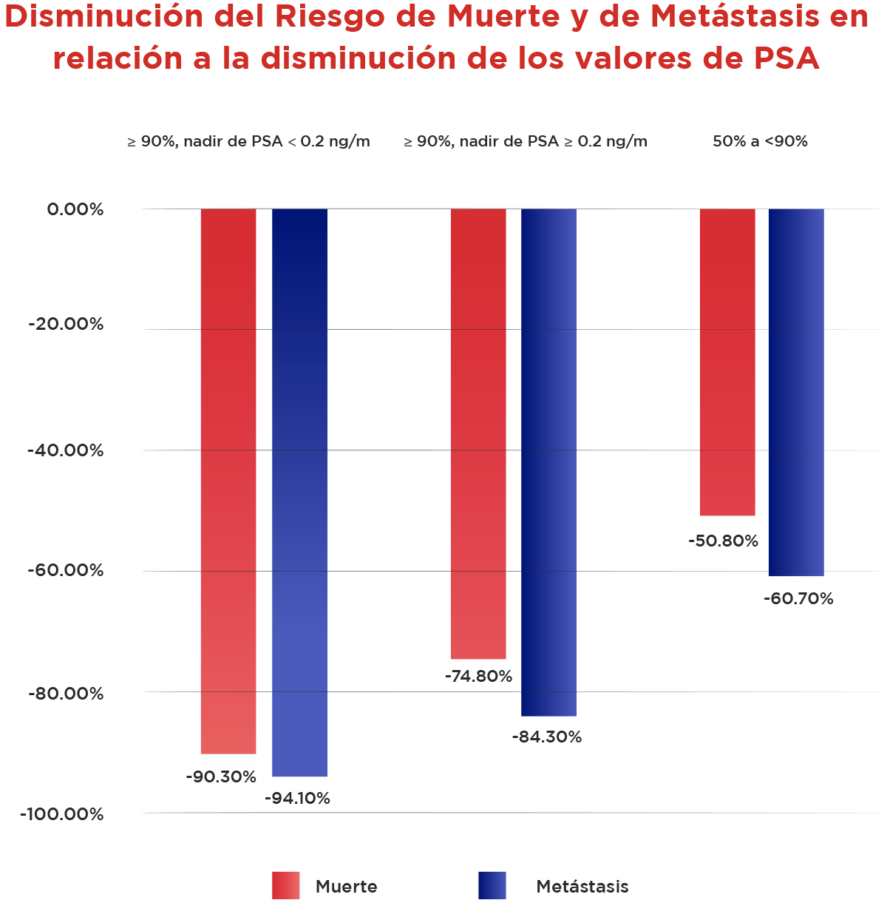
Lo anterior nos demuestra que la respuesta por PSA al usar enzalutamida en el escenario del cáncer de próstata resistente a la castración no metastásico, de acuerdo con la profundidad de respuesta puede asociarse a mejores resultados en cuánto a Supervivencia Global y Supervivencia Libre de Metástasis9.
Conclusiones
- El manejo de tamizaje puede aportar beneficio.
- La biopsia líquida cada vez muestra más beneficios en la evaluación del Cáncer de Próstata.
- No todas las combinaciones en el tratamiento del Cáncer de Próstata mostrarán beneficio; sin embargo, es un tema que abre un sinfín de oportunidades.
- Enzalutamida en estudios poblacionales demuestra mejor performance que flutamida.
- La profundidad de respuesta medida en los niveles de PSA en el uso de enzalutamida, se relacionan con mejoría en Supervivencia tanto Global como Libre de Metástasis.
Bibliografía
1.- Hugosson, J., Roobol, M., Månsson, M., Tammela, T., Zappa, M., & Nelen, V. et al. (2019). A 16-yr Follow-up of the European Randomized study of Screening for Prostate Cancer. European Urology, 76(1), 43-51. doi: 10.1016/j.eururo.2019.02.009
2.- Sharma, V., Venkataramana, A., Comulada, S., Litwin, M., & Saigal, C. (2021). Meeting Library | Meeting Library. Retrieved 17 February 2021, from https://meetinglibrary.asco.org/record/195181/abstract.
3.- Casanova-Salas, I., Athie, A., Boutros, P., Del Re, M., Miyamoto, D., & Pienta, K. et al. (2021). Quantitative and Qualitative Analysis of Blood-based Liquid Biopsies to Inform Clinical Decision-making in Prostate Cancer. European Urology. doi: 10.1016/j.eururo.2020.12.037.
4.- Tukachinsky, H., Madison, R., Chung, J., Dennis, L., Fendlerd, B., & Morley, S. et al. (2021). Meeting Library | Meeting Library. Retrieved 17 February 2021, from https://meetinglibrary.asco.org/record/195130/abstract
5.- Huebner, N., Shariat, S., Resch, I., Gust, K., & Kramer, G. (2020). The role of taxane-based chemotherapy in the treatment of prostate cancer. Current Opinion In Urology, 30(4), 527-533. doi: 10.1097/mou.0000000000000784.
6.- Rizzo, M. (2021). Mechanisms of docetaxel resistance in prostate cancer: The key role played by miRNAs. Biochimica Et Biophysica Acta (BBA) – Reviews On Cancer, 1875(1), 188481. doi: 10.1016/j.bbcan.2020.188481.
7.- Jones, R., Bahl, A., de Bono, J., Ralph, C., Elliot, T., & Robinson, A. et al. (2021). Meeting Library | Meeting Library. Retrieved 17 February 2021, from https://meetinglibrary.asco.org/record/194898/abstract.
8.- Uemara, H., Kobayashi, K., Yokomizo, A., Hinotsu, S., Horie, S., & Kakehi, Y. et al. (2021). Meeting Library | Meeting Library. Retrieved 17 February 2021, from https://meetinglibrary.asco.org/record/195077/abstract
9.- Hussain, M., Sternberg, C., Efstathiou, E., Fizazi, K., Shen, Q., & Lin, X. et al. (2021). Meeting Library | Meeting Library. Retrieved 17 February 2021, from https://meetinglibrary.asco.org/record/194913/abstract


Lo sentimos, el formulario de comentarios está cerrado en este momento.